JMLS 2019 June;4(1):1-13. http://jmls.or.kr Epub 2019 June 17
Copyright © 2019 by The Korean Society of Marine Life Science
Potential of Fucoidan Extracted from Seaweeds as an Adjuvant for Fish Vaccine
Eun Young Min; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea
Kwang Il Kim; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea
Mi Young Cho; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea
Sung-Hee Jung; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea
Hyun-Ja Han; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea
- Abstract
Fucoidan(후코이단)은 주로 갈조류에서 추출되는 fucose를 함유한 함황 다당류의 일종으로, 항균, 항바이러스 및 항종양 효과와 함께 다양한 경로로 면역력을 향상시키는 생리 기능성물질로 알려져 있다. 최근 연구에 따르면, 인체 백신 분야에서는 fucoidan의 백신 adjuvant(항원보조제)로서의 가능성이 제시되었다. 수산업 분야에서는, 보조사료로서의 fucoidan의 기능에 관한 연구는 보고되고 있으나, 수산용 백신 개발을 위한 adjuvant 연구는 전무한 실정이다. 동물세포에서 fucoidan의 adjuvant에 대한 긍정적인 검토와 함께 안전성을 증명한 연구는 많이 있지만, fucoidan을 어류 백신용 adjuvant로 사용하기 위해서는 어류에서도 이를 확인할 필요가 있다. 또한 fucoidan의 분자량에 따라 세포 내 흡수율이 각기 다르다는 점과 병원체의 인위감염에 따른 항체 생성을 포함한 어류의 특이면역 반응 시스템에 대한 연구가 많이 부족하다는 제약이 있다. 따라서 이러한 분야에 대한 적극적인 연구가 뒷받침 된다면 안전하고 효과적인 adjuvant로 사용할 수 있을 것이다. 본 연구에서는 fucoidan이 사람과 동물을 포함하여 어류의 면역자극 즉 체액성 및 세포성 면역에 미치는 영향에 대한 연구를 검토하고, 수산업 분야에서 fucoidan의 사용과 어류 백신용 adjuvant로서의 가능성을 고찰하였다.
Fucoidan is a physiologically functional ingredient extracted from seaweed brown algae, which is a sulfated polysaccharide containing fucose as a main molecule backbone. Fucoidan has a variety of immune-modulating or -stimulating effects, including promoting antigen uptake and enhancing anti-bacterial, anti-viral and anti-tumor effects. In addition, recent studies have suggested the possibility of use of fucoidan as a vaccine adjuvant in the field of human vaccine. Use of fucoidan as supplementary feeds have already been studied, but the development of fucoidan as an adjuvant of fish vaccine is still premature. However, the intracellular uptake of fucoidan differs depending on the molecular weight of fucoidan, and there is a limit to the study on specific immune response including the production of antibodies to fish caused by an artificial infection of pathogen. Although the safety of fucoidan has been demonstrated in animal cells, there is a need to confirm the safety of fucoidan in fish. Therefore, active research in this field is needed to use fucoidan as a vaccine adjuvant. This study discussed the effects of fucoidan on immune stimulation, humoral- and cellular- immunity including humans and animals. The prospect of fucoidan as a vaccine adjuvant in fisheries also reviewed.
Keywords: Fucoidan(후코이단) Brown seaweeds(갈조류) Fish vaccine(어류 백신) Adjuvant (항원보조제) Immune-stimulators(면역증강제)
Correspondence to: Hyun-Ja Han; Pathology Division, National Institute of Fisheries Science, Busan 46083, Korea; E-mail : jxheart@korea.kr
- Received
- 11 April 2019;
- Revised
- 23 April 2019;
- Accepted
- 4 June 2019.
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Language: Korean/English,
Full Text:

서 론
최근 들어 양식 어종의 편중화에 의한 가격 하락과 양식장 노후화 및 오염된 어장환경, 질병 발생 증가, 고수온 등의 자연재해로 인하여 국내 양식산업의 미래를 긍정적으로만 바라볼 수는 없다. 이로 인하여 정부는 지속 가능한 양식산업을 위한 친환경 양식정책을 추진하고자 노력하고 있다. 현재 양식산업에서 친환경 양식방법의 일환으로, 항생제 및 합성화학물질을 대체하기 위하여 질병을 예방할 수 있는 백신의 사용을 장려하고 있다(Hastein et al., 2005; Jung, 2006). 현재 양식현장에서는 백신투여 대상 품종이 대부분 넙치에 한정되어 있으며, 주로 주사법으로 백신을 사용하고 있다. 그러나 주사법은 어류, 특히 치어기에 상당한 스트레스를 유발하여 면역력을 저하를 초래할 뿐만 아니라 개체 접종에 따른 인건비 상승 및 장시간 소요 등의 단점이 있다. 이러한 주사법의 한계를 극복하기 위하여 수산용 경구 백신 및 백신의 장기 면역원성을 증가시키기 위한 adjuvant(항원보조제) 혼합 백신 연구 개발이 이루어지고 있다(Villumsen et al., 2015; Cho et al., 2017).
백신 개발에는 크게 유효 항원 개발, adjuvant, 백신전달 관련 기술이 필요하다. 그 동안은 약독화 생균, 복제 또는 비복제 병원체 및 subunits을 이용한 항원 개발 기술 위주로 이루어져 왔다. 생백신(live-attenuated)은 뛰어난 효과에 반해 부작용의 위험성을 최소화하는데 한계가 있어 보다 안전한 사백신(killed/inactivated)이나 병원균의 일부만을 사용하여 안전성이 월등한 subunit 백신으로 대체되는 추세이다. 양식산업에서도 생백신은 안전상의 이유로 사용 승인을 받지 못하는 경우가 있으며, 사백신은 자가복제가 불가능하고 정상적인 감염경로를 거치지 않기 때문에 백신의 효과가 상대적으로 감소될 수 밖에 없다. Subunit 백신도 사백신과 마찬가지로 정상적인 감염경로를 거치지 않는다는 점과, 미생물이 내재하고 있는 microbe-associated molecular patterns (MAMPs)을 가지고 있지 않기 때문에 그 자체만으로는 백신의 효과가 현저히 떨어진다는 단점이 있다. 따라서 아직 백신이 개발되지 않은 질병을 포함하여 고효능 백신 개량을 위해서는 보다 합리적인 접근방법으로 백신 설계 단계를 거쳐야 한다. 이에 따라 면역반응을 강화시킬 수 있는 백신 adjuvant의 필요성이 강력히 대두되었다(Pasquale et al., 2015). Adjuvant의 가장 중요한 요소는 백신의 효과를 극대화하고 안전성을 확보하는 것이며, 백신 제작 시 항원의 양을 감소시키더라도 면역효과는 유지되며, 추가 백신 접종 횟수를 줄여 백신 접종에 들어가는 시간과 비용을 절약할 수 있다면 더욱 좋은 후보물질이 될 수 있을 것이다. 일반적으로 백신에 의한 면역반응은 주로 항체성 반응으로, 항체에 반응하는 항원 부분이 T 세포에 비해 변이가 활발하다는 단점이 있다. 백신 접종 시 adjuvant를 사용하면 세포성 면역반응, 특히 T 세포성 면역반응을 더 효과적으로 유도하여 보다 광범위한 보호효과를 얻을 수 있다(Palm and Nedzhitov, 2009). 즉, 적합한 항원과 맞춤형 adjuvant 조합을 이용한다면 보다 효과적인 면역반응을 유도할 수 있는 백신 개발이 가능할 것이다.
어류 면역 체계에 대해서는 여전히 알려지지 않은 부분도 있지만, 22,000종의 어류도 "면역 특이성(immune peculiarities)"이 있어 선천성 면역(innate immunity)과 획득면역(adaptive immunity)으로 질병에 대항할 수 있다. 또한 현재 사용되는 대부분의 adjuvant는 농양형성, 장기손상 및 발열 등의 부작용이 발견되고 있어 효과적이고 새로운 백신 adjuvant의 필요성이 야기되고 있다(Stills, 2005). 따라서 본 논문에서는 수산용 백신 개발에 있어 fucoidan의 adjuvant로서의 가능성을 알아보기 위하여 수산용 vaccine adjuvant, 자연유래 물질인 fucoidan의 특징, 수산양식에서 fucoidan 사용 및 한계점 그리고 동물 백신에서의 활용 등도 함께 검토해보고자 한다.
1. 수산용 백신 adjuvant
최근 백신 연구 분야에서는 후천성 면역(adaptive immunity)만 연구하던 경향에서 벗어나 선천성 면역 시스템(innate immune system)이 염증반응을 일으키는 기전과 더불어 adaptive immune 조절반응에 대한 방향으로 확대되었다(Pulendran et al., 2011). 면역반응을 촉진시킬 수 있는 adjuvant의 주요 기전은 B-cell과 T-cell 등 다양한 경로를 통한 항원의 면역반응 향상, 혈중 내 항원의 잔류시간 증가, 항원 제시세포(antigen presenting cells)에 항원의 흡수 촉진, 대식세포(macrophage)와 임파구(lymphocyte)의 활성화 및 cytokines의 생성 촉진 등 이다(Marrack et al., 2009). 특히, Toll-like receptors (TLRs), pattern recognition receptors (PRRs)와 ligand인 MAMPs의 발견은 미생물에 의해 면역반응이 어떻게 시작되는지에 대한 결정적인 열쇠를 제공하였다(Pulendran et al., 2011). Adjuvant는 주로 사람을 대상으로 한 연구가 많이 진행되고 있으나, 상용화된 adjuvant의 상당량은 동물 백신용이며, aluminum hydroxide 또는 aluminum salts와 mineral oil이 주성분인 oil adjuvant가 가장 일반적이다(Park, 2008; Knight-Jones et al., 2014).
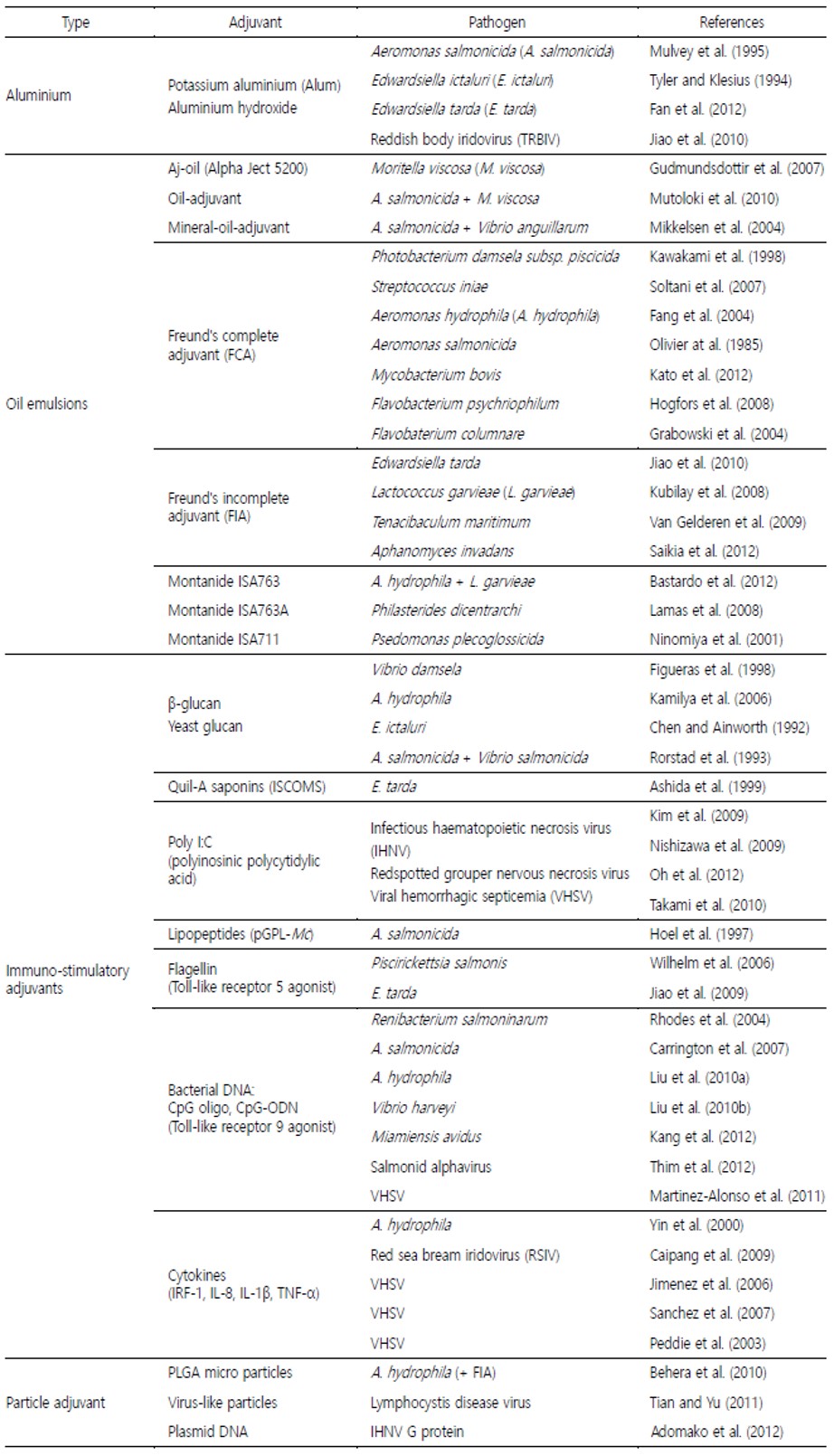
수산용 백신 adjuvant도 인체용 백신과 마찬가지로 항원 제시에 효과적인 종류와 B-cell 및 T-cell 활성에 따른 2차 추가 면역반응을 유도하는 종류로 구분할 수 있다. 항원 제시에 효과적인 adjuvant 종류로는 oil emulsion, Freund's complete (incomplete) adjuvant, Montanide, alum, nano- 또는 micro- 입자를 이용한 adjuvant, PLGA (Poly-lactide-co-glycolide)와 ISCOMs (Immune-stimulating complex) 및 기타 mineral oil adjuvants 등이 있다(Table 1). 대서양 연어(Salmo salar L.)와 농어(Dicentrarchus labrax)에서, 일부 상업용 mineral oil adjuvants는 비브리오병(vibriosis), 저수온기 비브리오병 및 절창병(furnculosis)과 같은 세균성 질병에 대하여 장기간 효과가 지속되는 것으로 나타났으나, 눈에 띄는 성장 지연과 육아종성 복막염 등과 같은 부작용이 있음이 밝혀졌다(Midtlyng et al., 1996; Midtlyng and Lillehaug, 1998; Afonso et al., 2005). 다른 종류의 adjuvant로는 면역증강제 또는 면역촉진제(immune-stimulants)의 일종으로, 알루미늄을 함유한 adjuvant나 Poly I:C (Polyinosinic polycytidylic acid), β-glucan, saponins, lipopeptides 및 cytokines 등이 있다(Table 1). 어류에서 비특이적 면역반응을 자극하는 것으로 알려진 β-glucan은 복강 주사 시, 용량 의존적으로 높은 항체 생성을 보였으며 adjuvant로서의 효과도 높은 것으로 보고되었다(Midtlyng et al., 1996; Ashida et al., 1999; Selvaraj et al., 2005; Kamilya et al., 2006). Saponine은 T1-helper와 T2-helper 반응을 자극 및 유도하는 특성이 있어 동물 백신 adjuvant로 많은 연구가 되고 있다(Sun et al., 2009). 가장 많이 사용되는 saponine의 종류로는 Quil-A가 있으나 높은 세포 독성과 수중에서의 불안전성으로 인해 다른 종류의 다양한 saponine이 adjuvant로 검토되고 있다(Ashida et al., 1999). Cytokine은 동물 백신에서 그 종류에 따라 많은 연구 결과가 있으나, 수산용 cytokine으로는 interleukin-8이 어류의 초기 면역반응을 조절할 수 있다는 점에서, 바이러스 백신 adjuvant로서의 잠재력이 탐색되고 그 가능성이 연구된 바 있다(Caipang et al., 2005; 2009).
Adjuvant는 백신의 효능을 향상시키는 기술로 정제된 단백질을 기본으로 합성 및 재조합 백신에 특히 중요하나, 앞서 언급한 oil adjuvant만 해도 많은 결함을 알면서도 사용하고 실정으로 아직 많은 연구가 필요한 분야이다. 최근에는 TLR ligand나 cytokine과 같은 adjuvant가 그 사용의 편리성으로 인해 oil adjuvant 대체제로 부각되고 있다. 면역세포는 병원체 감염 시, 각각의 병원성 세균이나 바이러스에 특이적인 면역반응을 일으키지만, 세균의 세포벽, lipopolysaccharide (LPS), 단백질이나 바이러스의 RNA/DNA와 같이 공통적으로 존재하는 분자들에 대응하기 위한 수용체를 가지고 있다. 이들을 pattern recognition receptor (PRR)이라고 하며, TLR은 대표적인 PRR이다. TLR agonist들은 면역세포에 대한 활성이 강하기 때문에 백신 adjuvant로서 개발되고 있다(Schnare et al., 2001). 경구 백신의 개발에서 중요한 부분이라 할 수 있는 점막 adjuvant는 점막세포에서 면역을 유도하기 위해 사용되며, 특히 subunit 백신을 점막 백신으로 개발하고자 할 때 유용하다. 대표적인 점막 adjuvant인 세균(Vibrio cholerae 등)의 B subunit 독소만을 분리하여 사용하면 세포 독성 없이 점막면역만을 활성화 할 수 있다. 독소의 B subunit은 표적세포의 수용체와 결합하여 A subunit이 세포로 들어갈 수 있도록 보조하며, A subunit는 세포 내에서 생리활성을 자극한다. 또한 리포좀(liposome)은 생체의 세포막과 같이 인지질의 이중막 구조를 가진 입자로 독성이 없으며, 그 자체로는 면역증강 활성이 없으나 양이온성 리포좀은 비특이적 면역활성이 있어 면역증강제로 개발되고 있다. 하지만 리포좀은 제조가 어려운 편이며, 동결 보관 시 쉽게 파괴되고, 냉장 보관 시에도 안전성이 낮다는 단점이 있다. 최근에는 두 종류의 TLR agonist를 같이 사용하거나 TLR4/TLR9 agonist를 alum 또는 리포좀과 함께 혼합하여 adjuvant로 개발하고 있다(Mount et al., 2013; Rombout et al., 2014). 앞으로 부작용을 줄이면서도 접종이 편리한 경구 백신의 개발을 위한 점막면역을 활성화 할 수 있는 adjuvant의 개발은 수산용 백신 개발에 있어 중요한 기술이라 할 수 있다.
2. Fucoidan 구조 및 특성
Fucoidan은 최근 천연 면역증강제로 인기를 얻고 있는 생리활성물질로 많은 연구들을 통해 항암, 항종양 효과, 항균, 항바이러스성, 항돌연변이 및 면역력 증강 등의 생리학적 효과가 구체적으로 확인됨에 따라, 특히 갈조류에 많이 포함되어 있는 fucoidan의 여러 기능성에 대한 관심이 높아졌다(Kwon et al., 2006; An et al., 2012; Lim, 2014; Kwak, 2014). 화학적 구조는 L-fucose에 에스테르화 황산을 주성분으로 하는 복합황산화 다당류로, 소량의 glucose, galactose, mannose, uronic acids 등과도 결합하고 있다(Choi et al., 2000). Fucoidan이란 이름이 동일한 구조의 물질을 의미하는 것은 아니며 주성분이 fucose인 고분자 다당류의 총칭으로 사용된다.
Fucoidan의 중요한 특징은 모든 천연 다당류가 다분산성(poly- dispersity)을 가지는 것과 마찬가지로 분자량이 다양하다는 것이다. 해조류 종류 또는 해조류의 발달 단계에 따라 다양한 구조를 보이는데 유사한 기후조건과 서식지에서는 유사한 구조를 가지는 것으로 알려져 있다(Cumashi et al., 2007; Skriptsova et al., 2010).
유럽 다시마(Saccharina latissima), 호스테일 켈프(Laminaria digitata), 헛가지말(Analipus japonicus), 큰실말(Cladosiphon okamuranus), 끈말(Chorda filum) 등에서 추출되는 fucoidan은 pyranose 잔기가 1→3 결합 구조로, 이 중 큰실말류(Cladosiphon sp.) 유래는 그 크기가 1927.2 kDa에 달한다. 뜸부기류(Ascophyllum nodosum)에서 추출되는 다당류는 α-L-fucopyranose 잔기가 1→3이 1→4로 변형된 구조이며(Imbs et al., 2011), 유럽 다시마(S. latissima) 유래 fucoidan은 395.4 kDa, 미역(Undaria pinnatifida)에서 추출된 것은 51.7 kDa에 달한다(Fitton et al., 2015). Fucoidan의 분자량에 따른 연구를 살펴보면, 뜸부기류(A. nodosum) 유래 fucoidan의 분자량은 500 kDa 이상의 고분자로, 그 자체로는 체내 흡수율이 낮기 때문에 저분자화하여 약리효과를 증대시킬 수 있다는 보고가 있으며(Alain et al., 1996), 다시마(Laminaria japonica) 유래 저분자 fucoidan이 항산화 및 항응고 효능이 높았다는 보고가 있다(Wang et al., 2010). 그러나 흥미로운 사실은 분자량이 712 kDa에 달하는 해조류(C. okamuranus, U. pinnatifida) 유래 fucoidan의 섭취 이후, 사람의 혈청과 소변에서 임상적으로 관찰되었다는 것이다(Irhimeh et al., 2005; Tokita et al., 2010). 이는 소화관 내의 산성조건에서도 fucoidan이 분해되지 않고 혈액 속으로 흡수되며 비록 소량이었으나 배출 직전의 소변에서도 fucoidan의 구조를 유지하고 있다는 것을 의미한다. 따라서 반드시 저분화된 fucoidan만이 면역효과가 있다는 것은 아니라는 것을 의미하기 때문에, 자연유래 fucoidan의 수산용 경구 백신 또는 면역증강제로서의 이용 가능성을 긍정적으로 검토할 수 있을 것이다.
3. 수산양식에서 fucoidan의 사용
양식생물에서 fucoidan의 투여효과에 대한 연구는 Table 2에서 볼 수 있듯이, 항산화 능력, 비특이적 면역반응 향상 및 질병 저항성을 증가시키는 사료 첨가제로서의 기능에 대한 보고가 대부분이다. 물론 추출 원료, 어종 및 발달 단계에 따라 fucoidan의 유효 농도는 다양하였으나, 적정 농도에서 사료 혼합 첨가 시, 면역증강 효과 및 어병 세균에 대한 저항성 증가를 보였다. Fucoidan의 세포 내 산화적 손상에 대한 저항 능력은 주로 free-radical 제거 능력, 지질과산화(lipid peroxidation), SOD (super oxide dismutase) 및 CAT (catalase) 같은 항산화(anti-oxidant) 효소를 측정함으로써 분석하였다. SOD는 CAT와 함께 세포 내에서 발생된 활성산소(ROS, reactive oxygen species)에 대한 첫 번째 방어선으로서, superoxide와 hydrogen peroxide를 제거하여 세포를 보호하는 역할을 한다(Hayes and McLellan, 1999).
Fucoidan의 면역증강 효과는 interleukin (IL)-1과 interferon-c의 생성을 유도하고 T-lymphocyte, B-cell, macrophage 및 병원성 감염세포를 파괴할 수 있는 자연살해세포(NK cells)의 기능 향상에 기인한다(Maruyama et al., 2006). 어류에서 fucoidan의 면역증강 효과를 검토한 연구에서는, 백혈구와 lysozyme의 활성, 식세포(phagocytes)의 호흡폭발(respiratory burst activity), 식균작용(phagocytosis) 그리고, 세균 및 바이러스에 대한 저항성 증가에 따른 폐사율 감소 등을 보고하면서 사료 첨가제 또는 면역보조제로서의 가능성을 제기하였다(Prabu et al., 2016). 새우류의 세균성 질병에 있어, 면역증강제 또는 사료 첨가제로서의 fucoidan의 가능성에 대한 검토는 여러 연구진들에 의해서 진행된 바 있다(Immanuel et al., 2012; Madasamy et al., 2014). 새우 사료에 fucoidan 첨가 시, 항균성과 phenoloxidase (PO), SOD 등의 증가로 인한 면역활성이 효과적으로 향상되었으며, 특히 WSSV (white spot syndrome virus) 항바이러스 활성에 대한 보고가 주를 이룬다(Takahashi et al., 1998; Chotigeat et al., 2004; Cruz-Suarez et al., 2007; Immanuel et al., 2010, 2012). 이상에서 볼 수 있듯이 fucoidan에 대해서 수산 분야에서는 아직까지 기능성 사료에 대한 검토만 이루어졌을 뿐, adjuvant로서의 가능성 연구는 미흡한 실정이다.
4. Adjuvant로서의 fucoidan의 가능성
이상적인 adjuvant는 병원균을 효과적으로 제거하기 위해서 안정된 구조여야 하며, 체액성 및 세포성 매개 면역반응을 활성화시키고, 독성은 낮은 생분해성이며 안전성도 보장되어야 한다(Aguilar and Rodrigues, 2007; Dubensky and Reed, 2010). 이런 점에서 fucoidan은 유망한 adjuvant 후보물질이라 할 수 있으며, 최근 이에 대한 연구가 빠르게 증가하고 있다(Kuznetsova et al., 2016). Fucoidan은 대식세포(macrophages)의 식균활성(phagocytosis) 증가, 자연살해세포(NK cells)의 활성 촉진으로 염증성 cytokines의 생성을 통한 항바이러스 작용과 CD4, CD8 T-cell에 의한 interferon 생산을 유도하여 cytotoxic T-cell을 통한 항균작용이 있음이 알려져 있다(Ale et al., 2011; Hayashi et al., 2008; Irhimeh et al., 2007; Kim and Joo, 2008). 또한, 쥐를 이용한 연구(in vivo)에서 fucoidan이 수지상 세포(dendritic cells)의 성숙, CTL의 활성화 및 Th1 면역반응을 통한 항원 특이적 항체 생산 및 memory T-cells 생성을 촉진시켜 adjuvant로서의 잠재성을 인정 받은 바 있다(Yang et al., 2006, 2008; Jin et al., 2009, 2014). 이러한 fucoidan의 효과는 수지상 세포(dendritic cells) 성숙의 전형적인 유도체인 종양괴사인자(TNF-α)의 효과와 유사하다는 것이 확인되었으며(Makarenkova et al., 2009), 이는 백신 항원에 대한 효과적인 면역기억을 확립하는데 중요한 역할을 한다.
돼지 호흡기 질환의 주요 원인균인 Bordetella bronchiseptica와 Mycoplasma hyopneumoniae 백신 개발 연구에서, adjuvant로 사용된 fucoidan은 항원 제시(antigen-presenting) 기능을 하는 MHC (major histocompatibility complex) class II의 발현을 자극하고, lymphocytes 활성화 표지자인 CD25 및 CD69의 발현을 매우 향상시켰다. 또한 B. bronchiseptica와 함께 투여한 경우 유의한 독성은 나타나지 않은 반면, 비장세포의 생존력과 백신의 유효성에 중요한 cytokine의 일종인 TNF-α의 생성을 유의하게 증가시키고, 발열반응을 초래할 수 있는 백신 항원의 농도를 낮출 수 있었다는 점에서, fucoidan의 adjuvant로서의 가능성을 보여주었다(Kim and Joo, 2015). 닭의 경우, 뉴캐슬병(newcastle disease), 전염성 기관지염 및 조류 인플루엔자에 대한 백신 접종 시, fucoidan을 adjuvant로 사용하였을 때, 백신 항원에 대한 체액성 및 세포성 매개 면역반응을 활성화시키는 효과를 보였다(Li et al., 2012). 인체의 경우, 인풀루엔자바이러스 A(H5N3 및 H7N2 subtypes)에 감염된 마우스 실험에서는 백신과 함께 fucoidan을 경구투여 시, 바이러스 복제 억제효과 및 호흡기 점막에서 국소적인 IgA 생성 증가와 높은 바이러스 중화 항체가를 보임으로 fucoidan의 adjuvant 효과가 입증되었다(Hayashi et al., 2013; Synytsya et al., 2014). 위에서 언급되었듯이 사람과 가축을 대상으로 한 연구에서 fucoidan의 adjuvant로서의 이용 가능성은 매우 긍정적으로 평가되고 있다.
결 론
해조류는 항균, 항바이러스, 항종양, 항혈액응고 및 면역력 증강 등의 생리적 순기능을 가진 것으로 밝혀졌다. 본 논문에서는 특히 갈조류에 많이 함유되어 있는 fucoidan의 항산화 효과, 면역증강 효과와 수산생물용 백신 adjuvant 후보물질로서의 가능성을 살펴보았다. 특히 fucoidan이 비장세포를 활성화하여 DC (dendritic cells)와 MHC class II의 발현을 증진시키는 등 항원 특이적 항체 생산을 향상시킨다는 점에서 그 가능성을 보여주었다. 하지만 fucoidan을 수산용 adjuvant로 사용하기까지는 극복해야 할 중요한 과제들이 남아있다. 예를 들어, fucoidan 투여 후, B-cell의 성숙도 및 비율 변화를 관찰한 연구에서 시험 농도 중 가장 높은 농도구(50 μg/ml)에서 오히려 B-cell 마커 발현이 감소하였다는 보고가 있다(Kim and Joo, 2015). 이는 lymphoblast에서 B-cell 마커 발현이 낮았기 때문일 수도 있으나, 어떤 기준 이상의 농도는 fucoidan과 관련된 세포 독성이 나타난 것일 수도 있기 때문에, 이 현상을 이해 및 극복하기 위해서는 어체 내 독성생리 반응에 대한 연구가 수행되어야 한다. 또한, 백신 적용 실험에서 어종에 따라서 가장 좋은 효과를 보이는 fucoidan의 최적 농도를 탐색하는 연구가 뒤따라야 할 것이다. Fucoidan은 in vitro 백신 실험에서는 면역증강 효과가 입증되었다고 볼 수 있다. 그러나 경구투여를 할 경우에는 백신 전달과정에서 위장관 벽이라는 한계가 있다는 점을 인지해야 한다. 일부 사람과 동물 연구에서, fucoidan을 경구 백신 adjuvant로 사용할 수 있음이 확인된 보고는 있다(Irhimeh et al., 2005; Tokita et al., 2010). 이 후, 장관 내 미생물에 의한 fucoidan의 분해 가능성도 제기되었으나(Kuznetsova et al., 2012), fucoidan이 소장 상피세포에서 일부 흡수된다는 사실이 확인되었다(Nagamine et al., 2015). Fucoidan은 분자량 및 구조적 특성에 따라 흡수율이 다르다고 보고되고 있다. 쥐의 비장세포에서, 고분자량 fucoidan(평균 130 kDa)은 세포의 생존력과 interferon-gamma와 nitric oxide를 증가시킨 반면, 저분자량(30 kDa)은 낮은 면역 활성과 비교적 높은 독성도 확인되었다(Jang et al., 2014). 그럼에도 불구하고, 저분자(4 kDa) 또는 나노 입자 형태의 fucoidan의 경우는 더 추가적인 연구가 필요하겠지만, 사람 및 동물 백신에서 adjuvant로서 전망이 밝다고 보고되었다(Lira et al., 2011; Lee et al., 2013).
백신은 수산생물의 질병을 예방하기 위한 매우 중요한 기술이라 할 수 있다. 특히 어류 질병을 효율적으로 제어하기 위해서는 특정 어류와 병원체를 대상으로 한 맞춤형 백신의 개발은 필수적이다. 현재까지 어류 백신은 세균성 질병에는 매우 성공적이었으나, 바이러스성 또는 진균 및 기생충성 질병에 대한 백신 개발은 아직까지 미진한 상황이다. 이러한 질병에 대응하기 위해서는 수산양식에 적용 가능한 DNA 백신, 재조합 백신 등 신규 기술 개발이 필요하다. 하지만 작용기전 연구, 유효성 연구, 안정성 확보에 이르기까지 그 개발 기간이 장시간 소요되는 기술 분야이며, 기초부터 개발 단계까지 장기적인 관점에서 계획할 필요가 있다. 그러나 수산용 백신 개발을 위하여 초기 연구 단계에서부터 진입한다는 것은 경제적인 관점에서도 어려운 점이 있기 때문에, 인체 또는 동물에서 개발한 백신이나 adjuvant를 도입하거나 공동 연구를 통하여 개발 기간을 단축시키고 개발 비용을 절감하는 것도 전략이라 할 수 있다. 특히 영국의 Patrick Smith 교수가 '경구 백신은 수산양식의 성배'라고 칭할 정도인(Smith, 2015) 경구 백신의 개발은 국내 수산양식산업에 재도약의 기회를 제공할 것이다.
- References
-
18. Cruz-Suarez LE, Hernandez J, Porchas-Cornejo M, Coronado-Molina DE, Limme-Unzueta-Bustamante ML, Nieto-Lopez M, Tapia-Salazar M, Ricque Marie D. 2007. Fucoidan extracted from the brown algae Cladosiphon okamuranus has been shown to be effective against WSSV in the white shrimp Litopenaeus vannamei. Aquaculture Asia Pacific 3: 19.
-
19. Cumahsi A, Ushakova NA, Preobrazhenskaya ME, D'Incecco A, Piccoli A, Totani L, Tinari N, Morozevich GE, Berman AE, Bilan MI. 2007. A comparative study of the anti-inflammatory, anticoagulant, antiangiogenic, and antiadhesive activities of nine different fucoidans form brown seaweeds. Glycobiology 17: 541-552.
-
109. Takahashi Y, Uehara K, Watanabe R, Okumura T, Yamashita T, Omura H, Yomo T, Kawano T, Kanemitsu A, Narasaka H, Suzuki N, Itami T. 1998. Efficacy of oral administration of fucoidan, a sulfated polysaccharide, in controlling white spot syndrome in Kuruma shrimp in Japan. In: Advances in Shrimp Biotechnology (ed. By T.W. Flegel), National center for genetic engineering and biotechnology, Bangkok, 1998, pp 171-173.
-
111. Thim HL, Illiev DB, Christie KE, Villonig S, McLoughlin MF, Strandskog G. 2012. Immunoprotective activity of a salmonid alphavirus vaccine: comparison of the immune response induced by inactivated whole virus antigen formulations based on CpG class B oligonucleotides and poly I:C alone or combined with an oil adjuvant. Vaccine 30: 4828-4834.